고세포 밀도 배양액에 대한 효율적인 중간 단계 심층 여과 방법
CHO 세포 기반의 고세포밀도(high cell density) 배양액에서도 안정적인 여과 성능을 구현할 수 있는 심층 여과 필터(depth filter) 조합을 찾고 계신가요? 본 연구에서는 두 가지 핵심 성능 지표인 탁도(turbidity) 감소와 처리량(throughput) 향상을 중심으로 필터 트레인(filter train)을 비교 평가하였으며, fed-batch 공정에서도 신뢰할 수 있는clarification 결과를 확인했습니다.
고세포밀도 조건에서도 안정적인 clarification 성능을 확보할 수 있는 심층 여과 필터(depth filter) 조합을 찾고 계시다면, 본 연구 결과를 통해 최적의 솔루션을 확인해보세요.
High Cell Density 배양액의 효율적인 Clarification을 위한 Depth Filter 트레인 비교 평가
최근 바이오의약품 산업에서는 fed-batch 방식의 세포 배양(fed-batch cell culture)에서 배양 용량은 감소하는 반면, 세포 밀도(cell density)와 항체 생산량(mAb titer)은 증가하는 추세입니다. 이러한 변화는 Clarification 단계에 부담을 가중시키며, 특히 Midstream 공정의 심층 여과(depth filtration)에서 중요한 도전 과제로 작용하고 있습니다.
세포 및 세포 잔여물(Cell debris)의 증가로 인해 기존 필터만으로는 미세 입자 제거(particle removal)에 한계가 있을 수 있으며, 미세 입자를 효과적으로 제거하기 위해 기존 필터 외에 대체 가능한 심층여과 솔루션을 고려해야 할 수도 있습니다.
이에 따라, Cytiva에서는 고세포밀도 배양액이라는 까다로운 조건에서 clarification 성능을 평가하기 위해 두 가지 심층여과 필터 트레인을 비교 분석했습니다.
- Train 1: CHO 배양에서 mAb 수확을 위해 특별히 설계된 Stax™ mAx 시스템으로, Primary 필터는 PDP8, Secondary 필터는 PDE2로 구성
- Train 2: Primary 필터는 PDK7, Secondary 필터는 PDCX로 구성
두 트레인 모두 고세포밀도 fed-batch 세포 배양액의 midstream clarification에서 우수한 결과를 보였습니다.
Train 2의 더 촘촘한 심층 여과 필터(depth filter)는 Train 1(9~13 NTU)에 비해 탁도가 낮은(3~4 NTU) 여과액을 생성하여 더 많은 미세 입자가 제거되었음을 보여주었습니다. 반면, Train 1은 더 높은 처리량(throughput)을 기록했습니다.
CHO 세포 기반 고세포밀도 배양액의 안정적 clarification을 위한 평가
mAb 공정 처리를 위한 Cytiva의 표준 옵션은 PDP8(coarse depth filter)와 PDE2(fine depth filter)로 구성된 Stax™ mAx 시스템입니다. 본 연구에서는 Train 1을 평가했으며, 더 촘촘한 구조의 조합인 PDK7과 PDCX depth filter로 구성된 Train 2도 함께 비교 분석하였습니다.
소규모 실험은 공정 개발을 위해 설계된 Supracap™ 50 depth filter 캡슐을 사용하여 수행되었으며, 이 캡슐은 다양한 depth filter media(여과재)의 시리즈 및 등급을 빠르고 정확하게 평가할 수 있도록 설계되었습니다. 또한, STAX™ 일회용 depth filter 시스템과 Supracap™ 100 시스템을 사용하여 선택된 심층 여과 미디어 기반의 scale-up 실험도 함께 진행되었습니다.
이러한 소규모 및 대규모 실험의 구성과 유효 여과 면적(effective filtration area, EFA)은 그래프 1에서 확인하실 수 있습니다.
그래프 1. Clarification의 1차 및 2차 단계에 사용된 사전 실험(pre-study) 및 대량 생산(main bulk processing)을 위한 심층 여과(depth filtration) 트레인 구성
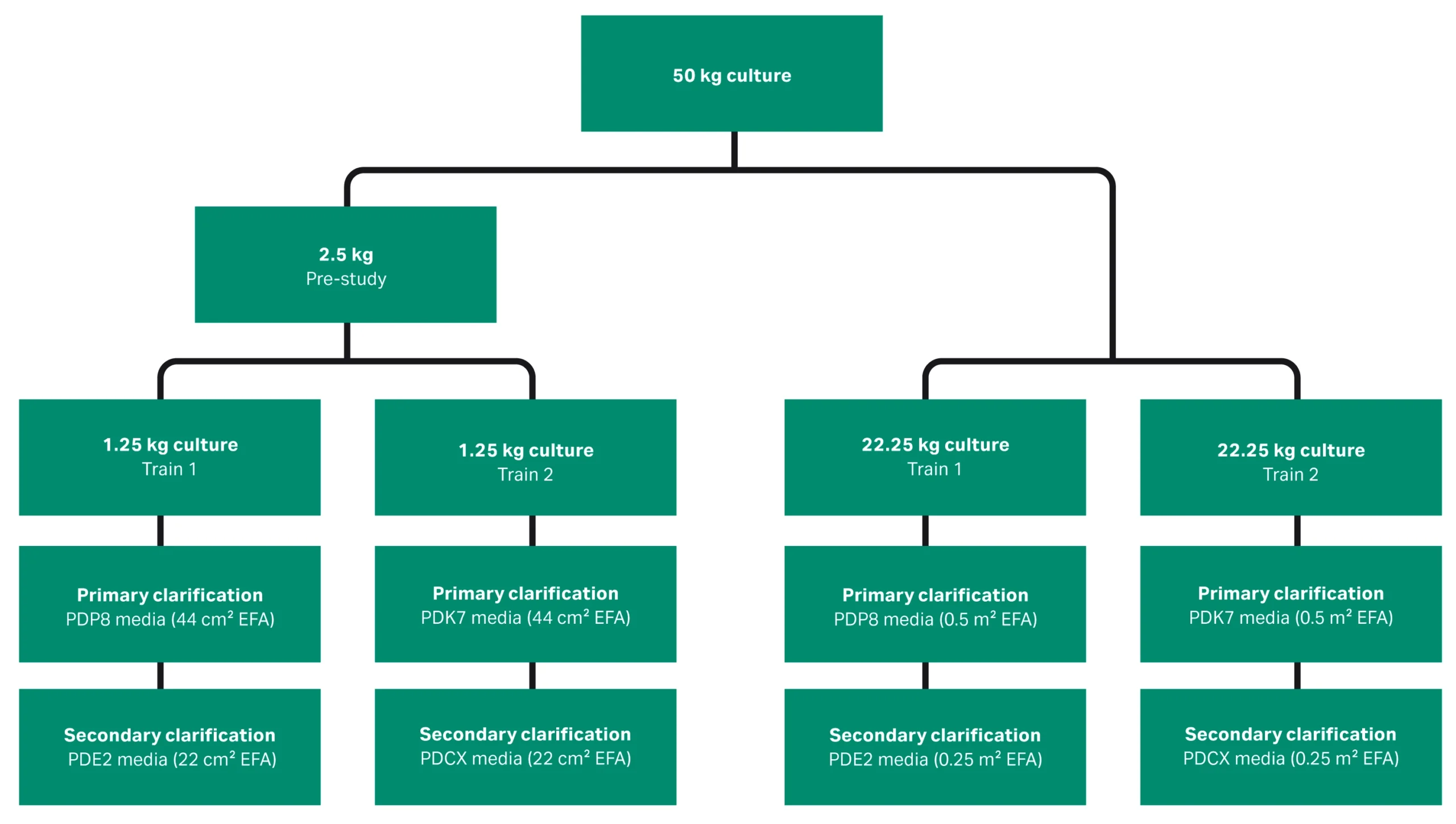
심층 여과 기반 clarification 공정의 실험 구성 및 조건
CHO 세포 기반 fed-batch 배양 공정
Xcellerex™ XDR-50 바이오리액터를 사용하여 50 L 규모의 CHO 세포 fed-batch 배양을 수행하였으며, HyClone™ ActiPro™ 배지와 Cell Boost™ 7a 및 7b 보충제를 통해 단일클론항체(mAb, monoclonal antibody)를 생산했습니다.
심층 여과를 통한 정제 전 처리 (Clarification using depth filtration)
수확 전, Supracap™ 50, Supracap™ 100, Stax™ depth filter 캡슐을 DI water로 세척하고 PBS(phosphate-buffered saline)로 프라이밍한 후, 제품 희석을 최소화하기 위해 배수(drain) 과정을 거쳤습니다. 전체 배양액 중 2.5 kg은 bench-scale(소규모 실험) 평가용으로 분리하였습니다
Depth Filtration 설정
- Train 1 (소규모): PDP8 Supracap™ 50 캡슐 2개를 병렬로 사용한 Primary filtration(44 cm²) 후, PDE2 Supracap™ 50 캡슐을 사용한 Secondary filtration(22 cm²)
- Train 2 (소규모): 동일한 캡슐 구성으로 PDK7과 PDCX media 사용
- Train 1 (대규모): PDP8 Stax™ M 캡슐(0.5 m²) 후 PDE2 Stax™ S 캡슐(0.25 m²)
- Train 2 (대규모): PDK7 Stax™ M 캡슐 후 PDCX Supracap™ 100 캡슐 20인치 2개 + 10인치 1개 병렬 사용 (총 0.25 m²)
1차 심층 여과(primary depth filter)에는 50 LMH(liters per square meter per hour), 2차 심층 여과(secondary depth filter)에는 100 LMH의 flux(유속)를 적용했습니다. 1차와 2차 clarification은 각각 별도로 수행되어 샘플링 및 탁도(turbidity) 측정이 가능하도록 구성되었습니다.
심층 여과(depth filtration)를 진행한 후, Supracap™ 50 depth filter를 통과한 여과액은 Supor™ EKV 멤브레인이 적용된 Mini Kleenpak™ 20 캡슐(20 cm²)을 통해 여과되었으며, 대량 여과액은 Kleenpak™ 캡슐(1500 cm²)을 통해 0.2 µm 멤브레인 여과(membrane filtration)를 수행하였습니다.
그래프 2. PDP8와 PDE2 또는 PDK7와 PDCX를 이용한 사전 연구에서의 심층여과 처리량
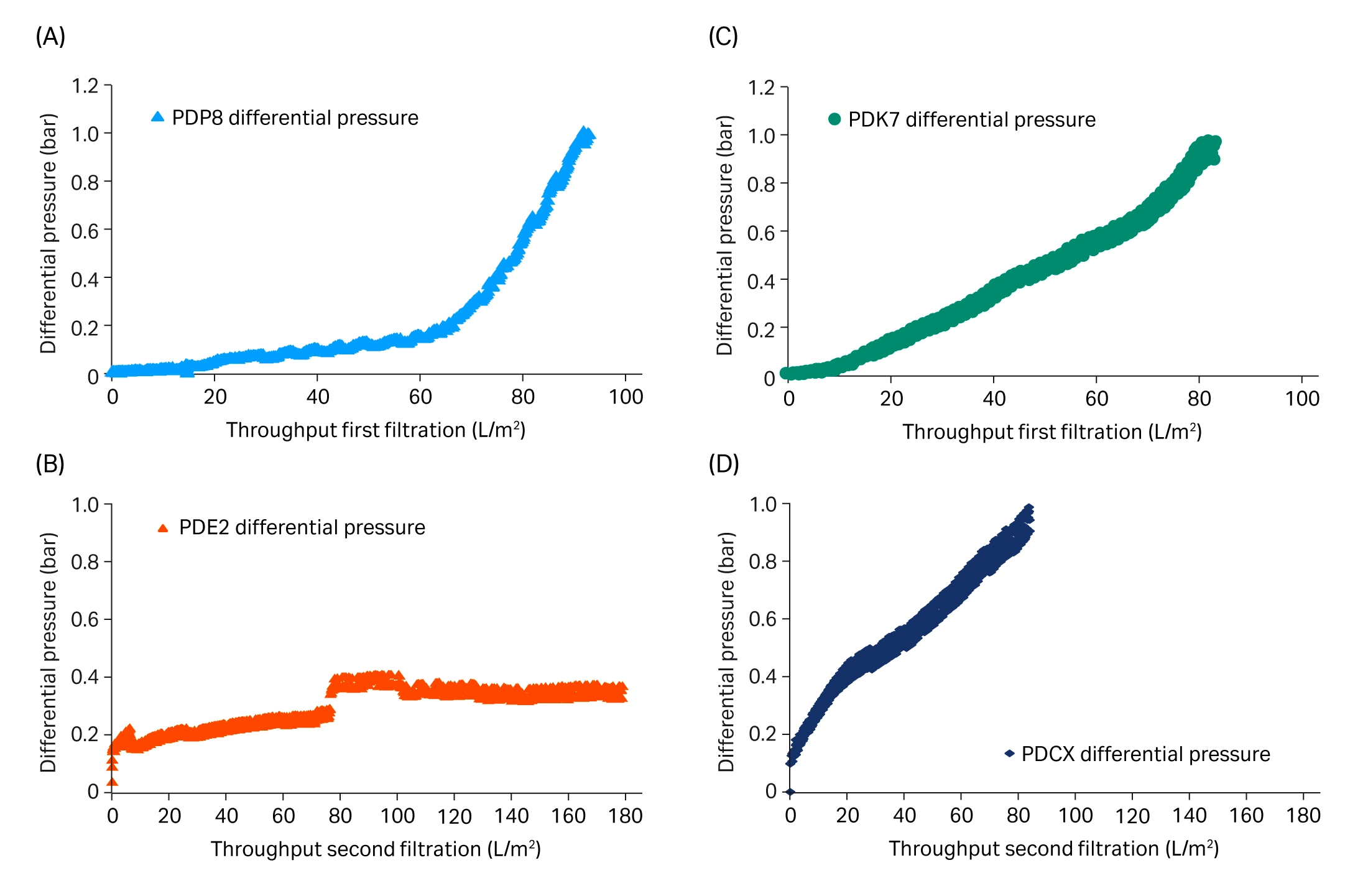
CHO 배양 및 Clarification 공정 성능 분석
CHO 세포 배양 특성
수확 시점의 CHO 배양은 다음과 같은 특성을 나타냈습니다.
- 생존율(Viability): 90%
- mAb 생산량(Titer): 3.8 mg/mL
- 최대 세포 밀도(Cell density): 36 × 10⁶ cells/mL
- 탁도(Turbidity): 2100 FNU
Clarification 공정 처리량 비교
Bench-scale 캡슐(Supracap™ 50)을 사용하여 두 트레인(Train 1, Train 2)의 처리 용량을 평가했습니다. 처리 용량(throughput)은 1.0 bar (0.1 MPa, 15 psi) 압력 차에서의 여과량으로 정의했습니다.
Pre-study Depth Filtration 결과
- PDP8 + PDE2 조합: 약 90 L/m² 및 >180 L/m²
- PDK7 + PDCX 조합: 약 85 L/m²
그래프 3. Supracap™ 50 format에서 수행한 사전 심층 여과 결과: Train 1(녹색)과 Train 2(주황색)
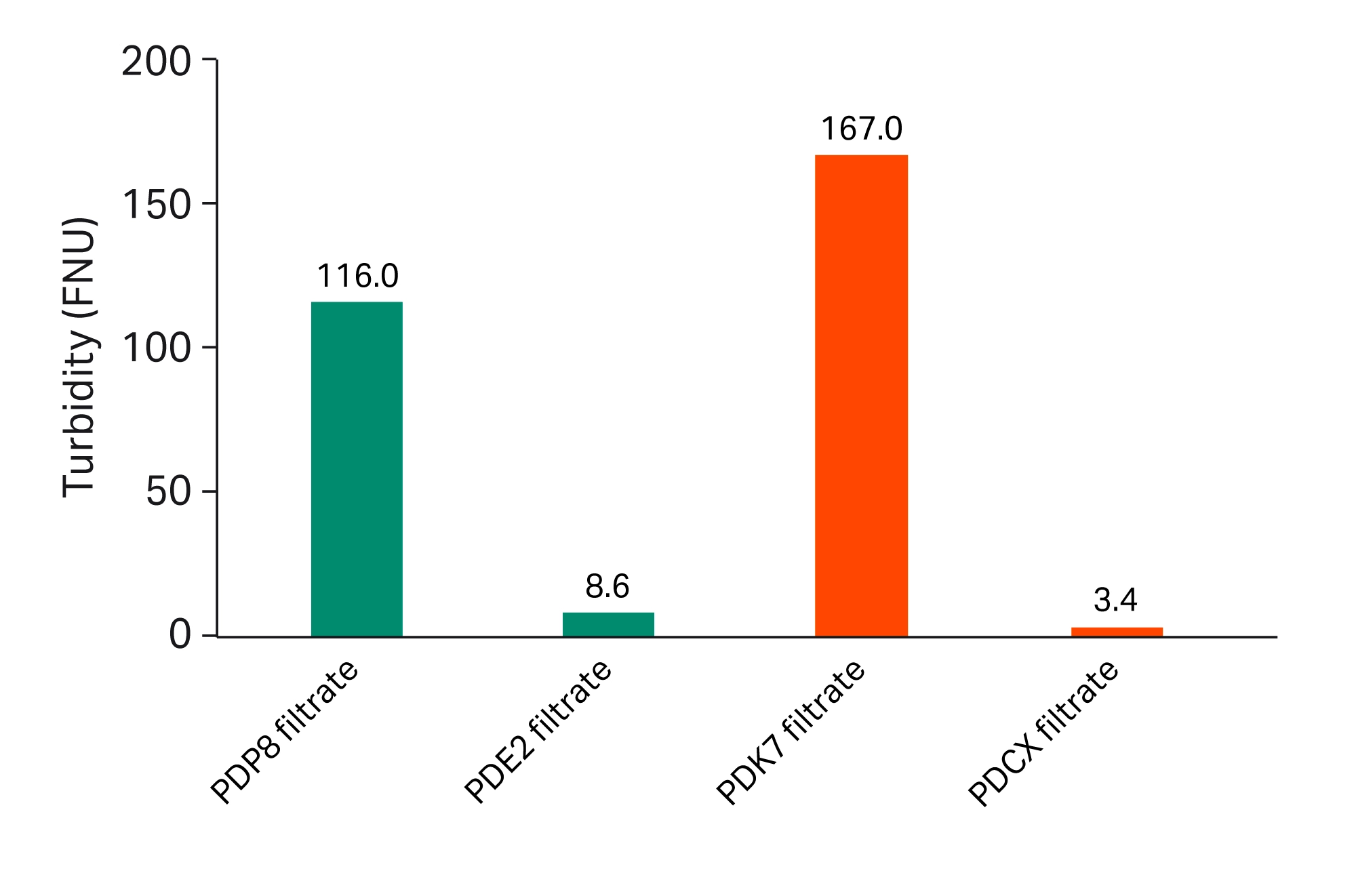
그래프 4. Stax™ 및 Supracap™ 100 format에서 수행한 메인 벌크 심층여과 (Main bulk depth filtration) 결과: Train 1(녹색), Train 2(주황색), 그리고 Supor™ EKV 여과 단계
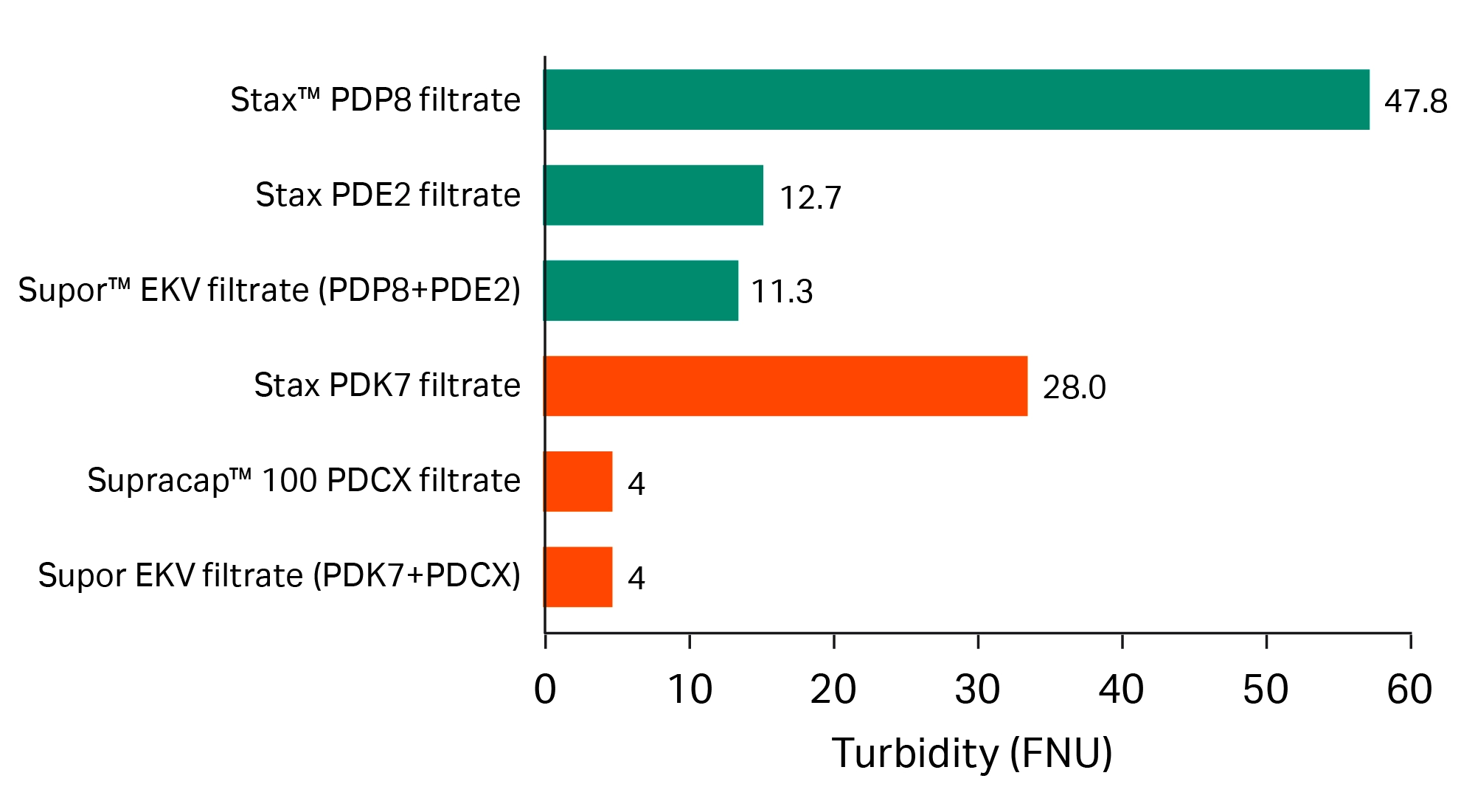
참고: Stax™ 캡슐은 Supracap™ 50 캡슐보다 낮은 탁도(turbidity)를 나타냈습니다. 이는 Stax™ 캡슐에 적용된 부하가 훨씬 낮았기 때문에 예상된 결과입니다.
Clarification Depth Filter 성능 요약 및 비교 결과
본 연구에서는 두 가지 depth filter 트레인을 Primary 및 Secondary clarification 용도로 테스트했습니다. 두 트레인 모두 fed-batch 방식의 High Cell Density CHO 배양액에서 midstream clarification 단계에서 우수한 성능을 보였습니다.
- PDK7 + PDCX 조합 → 더 낮은 탁도(turbidity) (3~4 NTU)
- PDP8 + PDE2 조합 → 더 높은 처리량(throughput)
이 결과는 고밀도 CHO 배양 공정에서 clarification 효율을 극대화하고, 최종 여과 단계의 품질 안정성을 확보하는 데 중요한 인사이트를 제공합니다. 고세포밀도 조건에서도 안정적인 clarification 성능을 제공하는 depth filter 조합을 찾고 계신다면, 지금 바로 전문가 상담을 신청하고 최적의 솔루션을 확인해 보세요.



